新形势下,药企抢占市场的关键就在临床试验。选择高质、高效的CRO公司,快速完成药物评价,将成为制药企业弯道超车的“制胜点”。


我们提供符合中美监管要求的双报BE整个流程的一站式外包服务:
医学调研与项目评估:对品种研发设计、风险与技术进行前期的充分调研和评估;生物等效性预试验(预BE):临床前处方筛选、体外-体内生物等效技术评估;
生物等效性试验(BE):方案设计、医学撰写、合作研究机构筛选、受试者招募、生物样品采集、生物样本分析检测、质量监查与稽查、数据管理与统计分析、临床总结报告、资料翻译和申报审评。
02服务优势
临床实施:提供灵活可靠的专业服务,执行高效的临床管理,为客户赢得时间和效益。以我们丰富的经验提供全面的建议方案,让风险更可控,BE一次通过率更高。临床资源丰富,多家战略合作机构,项目排期优先,确保进度。高效率交付项目,药品COA到位后2~3周内可以获得伦理批件,采血结束后2~3个月内交付申报资料,项目周期4个月达成。其中,承接的注射用伏立康唑PK对比临床研究(预实验4例+正式试验24例),8月开始预BE,10月交付正式试验总结报告,创下最短研究周期的记录。
样本检测:能够快速进行方法开发、方法验证和未知样本分析,测样结束后2~4周内交付检测报告。2020年12月,实验室首次通过国家局审核查验中心注册现场核查。2022年2月,承接的BE分析检测项目首次通过荷兰药物评价委员会(CBG)技术审评。2022年5月,零缺陷通过美国FDA的远程审计(Remote Record Review)。

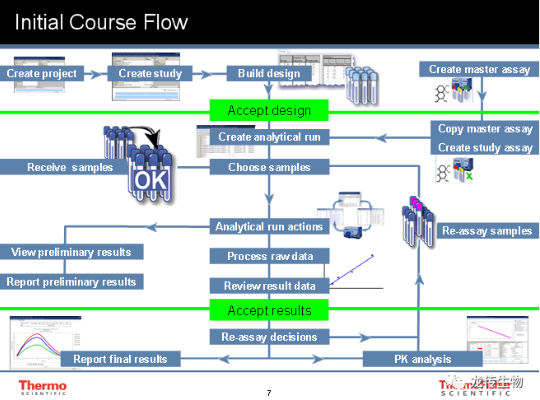
数据管理:提供多种多样的数据管理服务,根据项目需求,制定专属的数据管理方案。标准化、合规化的数据管理系统,试验全程精细的数据管理,保障每一个数据真实准确无误,充分满足临床试验审评申报要求。
统计分析:我们有独立的统计部门和生物统计学专家为临床试验项目提供全方位的统计学技术支撑。从临床前调研到方案设计,直至统计分析与报告全流程给予全程统计学技术支持,使整个试验科学性无可挑剔。
03双报项目经验
奥卡西平片(中欧)
伏立康唑干混悬剂(中美)
双氯芬酸钠缓释片(中欧)
利奈唑胺干混悬剂(中美)
阿奇霉素干混悬剂(中美)
磷酸奥司他韦胶囊(中美)
磷酸奥司他韦干混悬剂(中美)
马来酸曲美布汀片(中欧)
……


